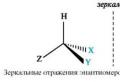
Хиральные молекулы. Хиральность и оптическая активность Хиральность в биологии
Энциклопедичный YouTube
1 / 5
✪ Примеры хиральности, часть 1
✪ Введение в хиральность
✪ Асимметрия биологических молекул - Максим Франк-Каменецкий
✪ Центры хиральности и стереоизомеры
✪ Тривиальные и систематические названия. Приставки «изо-», «втор-» и «трет-»
Субтитры
В прошлом видео мы узнали, что такое хиральная молекула, хиральный углерод или хиральный атом. В этом видео я хотел бы проработать ряд примеров и посмотреть, сможем ли мы определить хиральные атомы и распознать хиральные молекулы. Давайте посмотрим на наши примеры. Что у нас здесь? Это хлороциклопентан. Первый вопрос: видим ли мы здесь хиральные атомы? Давайте посмотрим на определение, которое мы дали хиральным атомам. Оно исходит из ситуации с направленностью рук и невозможностью их совмещения в зеркальном отражении. Мы также сказали, что обычно это атомы углерода, связанные с четырьмя разными группами. Посмотрим, есть ли у нас атомы углерода, связанные с четырьмя разными группами. Все CH2 соединены с другими CH2, а Н2 можно представить как H и H. Таким образом, они соединены с двумя H из той же группы, поэтому ни один из углеродов в CH2 не подходит на роль хирального центра или хирального углерода. Все они связаны с двумя водородами и двумя другими очень похожими группами CH2, даже если взглянуть на всю группу, с которой связан каждый углерод. Все они определённо связаны с двумя водородами, поэтому тут точно не может быть четырёх разных групп. Если мы посмотрим на CH, то увидим, что можем разделить его таким образом. Мы можем отделить от него H вот так. Помимо того что связан с водородом, этот углерод связан ещё и с хлором, а также с... Не совсем понятно, отличается ли эта группа от вот этой, если смотреть на схему с такой стороны. Но если подойти сбоку, если наполовину перевернуть её вот так. Или, может быть, лучше будет повернуть молекулу в этом направлении, против часовой стрелки. Тогда у нас есть группа CH2 и теперь ещё одна группа CH2. Затем третья такая группа и, наконец, четвёртая группа CH2. Возвращаемся, где были раньше. Итак, у нас есть 4 CH2, и мы можем вернуться. Что случится, если мы пойдём этим путём? У вас есть 1, 2, 3, 4 группы CH2, и вы возвращаетесь, откуда начали. Таким образом, это нижняя группа, ну, в зависимости от того, как далеко вы захотите её растянуть, и эта верхняя группа являются одинаковыми группами. Поэтому это не хиральный центр, не хиральный центр, или хиральный углерод. Он не связан с четырьмя различными группами. Также это не хиральная молекула, потому что у неё нет хирального центра. Как можно увидеть, что это не хиральная молекула? Посмотрим, что было написано ранее. Можно увидеть, что это не хиральная молекула. Существует несколько способов это понять. Простейший способ - это представить себе зеркальное отражение. Выглядеть оно будет примерно так. Здесь у нас зеркало, вот тут у нас хлор. Затем CH, CH2, CH2, потом CH2, CH2. Так мы завершаем наш циклопентан. Существует ли в такой ситуации способ повернуть это изображение, чтобы получить такое же? На что станет похожа молекула, если мы возьмём и просто перевернём её на 180 градусов? Ну может быть, немного меньше, чем 180 градусов, Да, не совсем 180, но если мы перевернём её так, чтобы хлор оказался вот здесь, у нас получится точно такая же молекула. Вот что у нас получилось. Выглядит немного по-другому. Вот так это будет выглядеть. Давайте попробуем сделать похоже. Примерно так. Здесь у нас CH2. Давайте лучше нарисуем здесь, тут у нас есть немного больше места. Если мы ее вот так переворачиваем, то здесь у нас CH. Здесь у нас хлор, затем - CH2 и все другие CH2, CH2. И, наконец, CH2 ещё вот тут сверху. Если мы перевернём её наоборот, точнее почти на 180 градусов, она будет выглядеть вот так. Единственная разница между этой и вот этой молекулой в том, как мы нарисовали эту связь. Вместо того чтобы рисовать её вниз мы можем нарисовать её вверх вот так, и у нас получится абсолютно такая же молекула. Так что эта молекула также не хиральная. Давайте перейдём к следующей молекуле. Что это такое? Это бромфторхлорметан - просто чтобы попрактиковаться немного в названиях. Совершенно очевидно, что здесь мы имеем дело с четырьмя разными группами. Каждая из этих групп, в данном случае атомов, которые связаны с углеродом, различны, поэтому углерод является хиральным центром. Хиральный центр. Также должно быть очевидно, что это хиральная молекула. Если мы сделаем её зеркальное отражение, очень похожее на пример из первого видео по хиральности, то зеркальное отражение будет выглядеть так. Теперь бром справа, водород будет по-прежнему снизу, а фтор наверху. Не имеет значения, как вы будете вращать эту молекулу. Если вы попробуете перенести бром сюда, на это место, тогда водород окажется в этом положении, а хлор будет вот в таком положении. Не имеет значения, как вы попытаетесь поворачивать её, вращать или перемещать, вы никогда не сможете совместить эту молекулу вот с этой молекулой. Так что это хиральный центр, и это хиральная молекула. Существует название для этих двух версий. Мы дадим им названия позже. Это другая тема. Будет отдельное видео на эту тему. Но вот эти 2 версии бромфторхлорметана, они иногда имеют различное химическое применение. Они называются энантиомерами. Энантиомеры - это зеркальные изображения. Каждая пара энантиомеров - это зеркальное отображение друг друга. Они являются стереоизомерами. Ну это просто терминология. Стереоизомеры. Вам знакомо слово «изомер», оно обозначает, что в нашей молекуле есть одинаковые атомы. Но существуют различные типы изомеров. Существуют структурные изомеры. Это означает, что разные элементы соединяются с разными элементами. Стереоизомеры - это когда каждый элемент соединён только с одним элементом. Углерод, соединяется только с фтором, хлор с углеродом, водород соединяется с углеродом, и бром соединяется с углеродом, то есть каждый элемент соединён с одним элементом, но они представлены в трёхмерной организации. Мы имеем дело со стереочастью. Стереохимия изучает трёхмерную химию как понимание сути реальной трёхмерной конфигурации вещей. Стереоизомеры подразумевают, что есть одинаковые компоненты, одинаковые атомы. Они одинаково связаны друг с другом. Бром связан с углеродом, который связан с водородом. Это все действительно так. Но их трёхмерное положение отличается. В данном случае, когда они являются зеркальным отражением друг друга, мы их называем энантиомерами. Здесь, наверное, стоит кое-что прояснить. В нескольких предыдущих видео мы употребляли слово «конфигурация», а иногда использовали слово «конформация». В некоторых случаях мы будем использовать «конфигурация», а в некоторых - «конформация». Этот момент следовало бы немного прояснить. Когда мы говорим о конфигурации, мы на самом деле говорим об иной структуре. Переходя от одной конфигурации к другой, мы разрушаем связи и в некотором роде пересобираем их. Вот что такое разные конфигурации. Для того чтобы они могли стать одинаковыми, нам, возможно, придётся поменять бром и водород там, где они связаны с углеродом. Вот это разные конфигурации. Конформации - это просто разные формы или разные ориентации одной и той же молекулы. Когда мы говорили о конформации ванны у циклогексана, то этот циклогексан в конформации ванны и этот же циклогексан в конформации кресла - это одна и та же молекула с одними и теми же связями. Мы не нарушали и не меняли никаких связей. Они просто оказались немного повёрнутыми. Так получились 2 разные конформации. А вот это -2 разные конфигурации. Чтобы перейти от одной к другой, нам придётся перестроить связи. Давайте посмотрим на эту молекулу. Можем ли мы увидеть здесь стереоцентры или хиральные углероды, или хиральные атомы? Вот здесь у нас есть углерод. Посмотрим: здесь углерод соединяется с хлором, водородом и бромом, а это другой углерод. Здесь есть соединения с четырьмя различными элементами, поэтому это хиральный углерод. Иногда здесь пишут маленькую звёздочку. Если посмотрим на этот углерод, то увидим, что он соединён с фтором и другим углеродом, но он также соединен с 2-мя водородами. поэтому он не хиральный. 2 из элементов, с которыми он соединён, - одинаковые. Здесь даже можно заметить небольшую ось симметрии, проходящую через него. Вы можете перевернуть его, и получится то же самое. Это хиральный центр. Хиральный центр, или хиральный углерод, или хиральный атом, или ассиметричный углерод. Мы увидим, что можно называть его по-разному. Благодаря тому что молекула имеет хиральный центр, это видно, если мы попробуем сделать зеркальное отражение, то получится энантиомер. Она не совмещаема со своим зеркальным отображением. Можно попробовать нарисовать её. Нет необходимости каждый раз рисовать зеркальное изображение справа. Мы можем нарисовать слева. Зеркальное отображение будет выглядеть так. Здесь фтор, углерод, углерод, хлор. Здесь получаются 2 водорода, затем ещё 1 водород здесь, и вот здесь у нас будет бром. Неважно, будете вы переворачивать молекулы или делать что-то еще, вы никогда не сможете ее совместить вот с этой, поэтому здесь у нас 2 энантиомера. Они оба являются стереоизомерами по отношению друг к другу. И каждый из них является хиральной молекулой. Сейчас у нас уже заканчивается время, которое обычно отводится на видео, поэтому мы продолжим в следующем видео и постараемся успеть больше.
История
Хиральность молекул была открыта Л. Пастером в 1848 году. Пастер обратил внимание на то, что кристаллы, выпадающие из раствора рацемического тартрата натрия -аммония , имеют две формы, представляющие собой зеркальные отражения, которые не совмещаются друг с другом в пространстве. Напротив, кристаллы индивидуального правовращающего тартрата натрия-аммония имели одинаковую форму с малыми плоскостями, направленными в одну сторону. Пастер провёл подобные кристаллизации с тринадцатью энантиомерно чистыми соединениями (различными тартратами и винной кислотой), а также с шестью рацемическими тартратами и сделал вывод о существовании хиральности молекул и объяснил ранее неизвестный вид изомерии винных кислот - энантиомерию .
Структурная трактовка хиральности стала возможной после введения в 1874 году Я. Вант-Гоффом и Ж. Ле Белем концепции асимметрического атома углерода, то есть тетраэдрического атома углерода с четырьмя различными заместителями .
Понятие хиральности было введено лордом Кельвином в конце XIX в.
Я называю какую-либо геометрическую фигуру, или группу точек, хиральной и говорю, что она обладает хиральностью, если её изображение в идеальном плоском зеркале не может быть с ней совмещено.
Оригинальный текст (англ.)
I call any geometrical figure, or group of points, chiral, and say it has chirality, if its image in a plane mirror, ideally realized, cannot be brought to coincide with itself.
У. Т. Кельвин. Балтиморские лекции по молекулярной динамике и волновой теории света, 1904
Симметрия хиральных молекул
Виды хиральности
В зависимости от элемента молекулы, наличие которого приводит к возникновению хиральности, различают следующие виды хиральности:
Центральная хиральность
Основная статья: Центральная хиральность
Центральная хиральность возникает в результате наличия в молекуле центра хиральности (хирального центра), которым, как правило, является асимметрический атом углерода , имеющий 4 различных заместителя. Хиральными центрами могут быть также атомы , , , реже - . В хиральных производных адамантана центр хиральности находится в середине углеродного каркаса, где атомов нет вовсе .
Аксиальная (осевая) хиральность
Основная статья: Аксиальная хиральность
Аксиальная хиральность возникает в результате неплоского расположения заместителей относительно некоторой оси - оси хиральности . Ось хиральности существует в несимметрично замещённых алленах. sp -гибридный атом углерода в аллене имеет две взаимно перпендикулярные p -орбитали. Их перекрывание с p -орбиталями соседних атомов углерода приводит к тому, что заместители в аллене лежат во взаимно перпендикулярных плоскостях. Подобная ситуация наблюдается также в замещённых бифенилах , в которых вращение вокруг связи, соединяющей ароматические кольца , затруднено, а также в спироциклических соединениях.
Планарная хиральность
Основная статья: Планарная хиральность
Плоскость хиральности присутствует в производных ферроцена , замещённых парациклофанах и др. При помощи данного термина описывают хиральное расположение внеплоскостных элементов молекулы относительно плоскости хиральности .
Спиральная хиральность
Спиральная хиральность характерна для соединений, имеющих элементы в форме спирали, пропеллера или винта, например для гелиценов . Шесть ароматических колец в гексагелицене не могут уложиться в одной плоскости, поэтому образовывают спираль, которая может быть закручена влево или вправо. Данный вид хиральности наблюдается также в белках и нуклеиновых кислотах .
Топологическая хиральность
Топологическая хиральность связана с наличием структурной несимметричности, характерной для супрамолекул , например, катенанов , ротаксанов , молекулярных узлов .
Хиральность соединений со стереогенной парой электронов
Хиральность в биологии
Многие биологически активные молекулы обладают хиральностью, причём природные аминокислоты и сахара представлены в природе преимущественно в виде одного из энантиомеров : аминокислоты, в основном, имеют l -конфигурацию, а сахара - d -конфигурацию .
Две энантиомерные формы одной молекулы обычно имеют различную биологическую активность. Это связано с тем, что рецепторы , ферменты , антитела и другие элементы организма также обладают хиральностью, и структурное несоответствие между этими элементами и хиральными молекулами препятствует их взаимодействию. Например, ферменты , являющиеся хиральными молекулами, часто проявляют специфическую реакционную способность по отношению к одному из энантиомеров. Подобные примеры характерны и для лекарственных соединений. Так, биологической активностью обладает лишь один энантиомер ибупрофена - (S )-(+)-ибупрофен, в то время как его оптический антипод (R )-(−)-ибупрофен в организме неактивен .
Гомохиральность
Основная статья: Гомохиральность
За редкими исключениями, природные хиральные аминокислоты и моносахариды представлены в виде единственного изомера из двух возможных. Так, в состав белков входят практически исключительно l -аминокислоты, а ДНК и РНК построены только на основе d -углеводов . Данное свойство химических соединений называется гомохиральностью (хиральной чистотой). Происхождение и назначение данного явления до конца не установлены, однако его часто связывают с проблемой происхождения жизни .
Молекулы, обладающие одинаковым химическим строением, могут различаться пространственным строением, т.е. существовать в виде пространственных изомеров - стереоизомеров .
Пространственное строение молекул - это взаимное расположение атомов и атомных групп в трехмерном пространстве.
Стереоизомеры - соединения, в молекулах которых имеется одинаковая последовательность химических связей атомов, но различное расположение этих атомов относительно друг друга в пространстве.
В свою очередь стереоизомеры могут быть конфигурационными и конформационными изомерами , т. е. различаться соответственно конфи- гурацией и конформацией.
Конфигурация - это порядок расположения атомов в пространстве без учета различий, возникающих вследствие вращения вокруг одинарных связей.
Конфигурационные изомеры могут переходить друг в друга путем разрыва одних и образования других химических связей и могут существовать раздельно в виде индивидуальных соединений. Они подразделяются на два основных типа - энантиомерыи диастереомеры.
Энантиомеры - стереоизомеры, относящиеся друг к другу, как предмет и несовместимое с ним зеркальное отображение.
В виде энантиомеров могут существовать только хиральные молекулы.
Хиральность - это свойство объекта быть несовместимым со своим зеркальным отражением. Хиральными (от греч. cheir - рука), или асимметричными, объектами являются левая и правая рука, а также перчатки, ботинки и др. Эти парные предметы представляют собой объект и его зеркальное отражение (рис. 8, а). Такие предметы не могут быть полностью совмещены друг с другом.
В то же время существует множество окружающих нас предметов, которые совместимы со своим зеркальным отражением, т. е. они являются ахиральными(симметричными), например тарелки, ложки, стаканы и т. д. Ахиральные предметы обладают, по крайней мере одной плоскостью симметрии, которая делит объект на две зеркально-идентичные части (см. рис. 8, б ).
Подобные взаимоотношения наблюдаются также в мире молекул, т. е. молекулы делятся на хиральные и ахиральные. У ахиральных молекул есть плоскости симметрии, у хиральных их нет.
В хиральных молекулах имеется один или несколько центров хиральности. В органических соединениях в качестве центра хиральности чаще всего выступает асимметрический атом углерода.
Рис. 8. Отражение в зеркале хирального объекта (а) и плоскость симметрии, разрезающая ахиральный объект (б)
Асимметрическим является атом углерода, связанный с четырьмя различными атомами или группами.
При изображении стереохимической формулы молекулы символ «С» асимметрического атома углерода обычно опускается.

Чтобы определить, является молекула хиральной или ахиральной, нет необходимости изображать ее стереохимической формулой, достаточно внимательно рассмотреть все атомы углерода в ней. Если находится хотя бы один атом углерода с четырьмя разными заместителями, то этот атом углерода асимметричен и молекула за редкими исключениями хиральна. Так, из двух спиртов - пропанола-2 и бутанола-2 - первый ахирален (две группы СН 3 у атома С-2), а второй - хирален, так как в его молекуле у атома С-2 все четыре заместителя разные (Н, ОН, СН 3 и С 2 Н 5). Асимметрический атом углерода иногда помечают звездочкой (С*).

Следовательно, молекула бутанола-2 способна существовать в виде пары энантиомеров, которые не совмещаются в пространстве (рис. 9).

Рис. 9. Энантиомеры хиральных молекул бутанола-2 не совмещаются
Свойства энантиомеров. Энантиомеры обладают одинаковыми химическими и физическими свойствами (температуры плавления и кипения, плотность, растворимость и т. д.), но проявляют различную оптическую активность,т. е. способность отклонять плоскость поляризованного света.
При прохождении такого света через раствор одного из энантиомеров происходит отклонение плоскости поляризации влево, другого - вправо на один тот же по величине угол α. Значение угла α, приведенное к стандартным условиям, является константой оптически активного вещества и называется удельным вращением [α]. Левое вращение обозначается знаком «минус» (-), правое - знаком «плюс» (+), а энантиомеры называют соответственно лево- и правовращающими.
С проявлением оптической активности связаны другие названия энантиомеров - оптические изомеры или оптические антиподы.
Каждое хиральное соединение может иметь и третью, оптически неактивную форму - рацемат . Для кристаллических веществ это обычно не просто механическая смесь кристаллов двух энантиомеров, а новая молекулярная структура, образованная энантиомерами. Рацематы оптически неактивны, так как левое вращение одного энантиомера компенсируется правым вращением равного количества другого. В этом случае перед названием соединения иногда ставят знак «плюс-минус» (?).
Стереоизомеры, их виды
Определение 1
Стереоизомеры – это вещества, в молекулах которых атомы связаны между собой одинаково, но расположение их в пространстве различно.
Стереоизомеры подразделяют на:
- Энантиомеры (оптические изомеры). Имеют одинаковые физико – химические свойства (плотность, температуру кипения и плавления, растворимость, спектральные свойства) в ахиральном окружении, но различную оптическую активность.
- Диастеромеры – это соединения, которые могут содержать два и более хиральных центра.
Под хиральностью понимают способность объекта не соответствовать своему зеркальному отражению. То есть, молекулы, не обладающие зеркально – поворотной симметрией, являются хиральными.
Определение 2
Прохиральная молекула – это молекула, которая может быть превращена в хиральную единственным изменением любого ее фрагмента.
В хиральных и прохиральных молекулах некоторые группы ядер, на первый взгляд химически эквивалентные, являются магнитно неэквивалентными, что подтверждают спектры ядерного магнитного резонанса. Это явление называется диастереотопией ядер, может наблюдаться по спектрам ядерного магнитного резонанса при наличии в одной молекуле прохирального и хирального фрагментов.
Например, в прохиральной молекуле две группы OPF2 являются эквивалентными, но в каждой группе атомов $PF_2$ атомы фтора неэквивалентны.
Это проявляется в константе спин – спинового взаимодействия 2/$FF$.
Если молекула оптически активная , то неэквивалентность ядер Х в тетраэдрических группах –$MX_2Y$ (например, -$CH_2R$, -$SiH_2R$ и др.) или пирамидальных группах –$MX_2$ (например, -$PF_2$, -$NH_2$ и др.) не зависит от высоты барьера внутреннего вращения этих групп. При вращении плоских групп –$MX_2$ и тетраэдрических –$MX_3$ потенциальный барьер очень низок, в результате чего ядра $X$ становятся эквивалентными.
Построение названий хиральных молекул
Современная система построения названий для хиральных молекул предложена Ингольдом, Каном и Прелогом. Согласно этой системе, для всех возможных групп $A$, $B$, $C$, $D$ при асимметричном атоме углерода выясняется порядок старшинства. Чем больше атомный номер, тем он старше:
Если атомы одинаковые, то сравнивают второе окружение:
Предположим, что группы расположены по уменьшению старшинства: $A → B → C → D$. Развернем молекулу таким образом, чтобы младший заместитель $D$ был направлен за плоскость рисунка, от нас. Тогда понижение старшинства в остальных группах может происходить либо по часовой, либо против часовой стрелки.
Замечание 1
Если понижение старшинства происходит по часовой стрелке при обозначении изомера используют символ $R$ (правый), если против часовой стрелки – $S$ (левый). Понятия «левый» и «правый» не отражают реального направления вращения линейно поляризованного света.
Эмиль Фишер предложил $DL$ –номенклатуру, согласно которой правовращающийся энантиомер обозначается буквой $D$, а левовращающийся – $L$. Эта номенклатура широко используется для обозначения аминокислот и углеводов.
Стереоспецифичность физиологической активности оптических изомеров
Оптические изомеры проявляют разную физиологическую активность. Активные центры ферментов и рецепторы состоят из аминокислотных остатков, которые являются оптически активными элементами.
Рецептор распознает физиологически активную молекулу по принципу «ключ в замке». При присоединении молекулы субстрата, активный центр меняет свою геометрию.
Например, никотиновый алкалоид содержит один центр оптической изомерии и может существовать в виде двух энантиомеров. $S$ - изомер расположен справа и является ядом для человека (летальная доза 20 мг), $R$- изомер менее ядовит:
$L$ – глутаминовую кислоту
широко используют в качестве усилителя вкуса мяса при приготовлении консервов. $D$ - глутаминовая кислота такими свойствами не обладает.
В соединении
есть два асимметричных атома углерода, следовательно, возможно существование 4 изомеров ($2^n$). Но только один ($R,R$)-изомер – хлоромицетин - проявляет свойства антибиотика
Получение чистых оптических изомеров является важной химико – технологической проблемой.
Пути получения чистых энантиомеров.
Хиральность - это способность объекта существовать в двух зеркально-симметричных формах, например, как левая и правая ладони. Научные исследования показывают, что каким-то образом разделение на "лево" и "право" является обязательным условием существования жизни! Ведь хиральность присуща не только материальным объектам, но и молекулам. Это явление было открыто в середине XIX века Луи Пастером, который исследовал химическую асимметрию цитоплазмы живых клеток.
Как известно, органические молекулы содержат в себе большое число различных атомов и имеют пространственную структуру. Иногда одни и те же атомы могут располагаться в теле молекулы различным образом. Это называется изомерия. А зеркально-симметричные формы изомеров, одинаковые, но как бы закрученные в разные стороны, называются энантиомерами . От того, в какую сторону вращается молекула, полностью зависят свойства вещества, они по-разному вступают в реакции и взаимодействуют с другими веществами, особенно биологическими, а как лекарства имеют различные эффекты.
Например, энантиомеры вращают в разные стороны плоскость поляризации света при прохождении его через раствор. Кстати, по направлению вращения плоскости поляризации их и разделяют на L-формы (или S-формы, лево-вращающие) и D-формы (или R-формы, право-вращающие). Другие примеры явлений, в которых непосредственно проявляет себя явление хиральности, - это хроматография и электрофорез. Ещё большую роль хиральность играет в жизнедеятельности и развитии живых организмов, формировании симметрии их тел, процессах деления клеток и развитии зародыша. Так, L–листья фасоли превосходят D–листья по интенсивности фотосинтеза и дыхания, а также по содержанию пигментов (хлорофиллов a и b, лютеина, виолоксантина и каротина), и обладают также большей засухо– и жароустойчивостью. Микроорганизмы образуют колонии только определённой (L или D) спиральной структуры. Подавляющее большинство раковин моллюсков также закручены влево (L).
Всем неживым системам присуща обычная симметрия, а живым - зеркальная. Все органические соединения способны образовывать энантиомеры, но только один из этих энантиомеров ("левый" или "правый") способен поддерживать жизнь. Поэтому все рецепторы, ферменты, гормоны, антитела и прочие элементы организма присутствуют в организмах только в одной из своих зеркально-симметричных форм. Так, все сахара (углеводы), нуклеотиды, ДНК и РНК имеют D-конфигурацию, а все молекулы ферментов, аминокислот и белков - L-конфигурацию.
Биологи без преувеличения утверждают, что хиральность является тем необходимым свойством материи, которое даёт ей жизнь. Но существование всех биологических веществ в природе только в одной своей хиральной форме ставит жирный крест на Теории Эволюции. Ведь вероятность образования даже сравнительно небольшого протеина из 100 аминокислот только L-конфигурации составляет "два в минус сотой степени" или "десять в минус тридцатой"! При этом происхождение хиральности остаётся полной загадкой, и у науки нет никакого ответа на вопрос, почему в природе остались только L или D изомеры, а их энантиомеры полностью исчезли.
Хиральность имеет решающее значение при создании лекарств. Если синтезировать в лабораторных условиях какое-либо сложное органическое вещество, то получится так называемая рацемическая смесь , в составе которой в равных количествах будут присутствовать L и D-изомеры. Поскольку их биохимические свойства различны, фармацевты вынуждены отделять энантиомеры друг от друга. Так, только S-форма ибупрофена обладает антивоспалительным действием, его R-форма неактивна. Другой пример: только L-тироксин является гормоном щитовидной железы человека, а его D-форма - опасное токсичное вещество.
Последние исследования раковых клеток показало, что в них наблюдается повышенное содержание энзима изомеразы (AMACR), которая ответственна за хиральную инверсию - превращение "мёртвых" энантиомеров в "живые". Поэтому биологи называют одной из причин раковых заболеваний - употребление неправильных энантиомеров: искусственно синтезированных сахаров, жиров и вкусовых добавок, которые по сути являются рацемическими смесями. Ещё один пример: лишь направление вращения отличает искусственно созданный в лабораторных условиях D-никотин от всем известного L-никотина, который входит в состав любого табака, но если первое соединение нейтрально для организма человека, то по раковым заболеваниям лёгких уверено лидируют курильщики.
 Интересно, что явление хиральности отражено в древних учениях об организме человека. Так, в системе йоги указано на существование в теле человека трёх каналов - левого, правого и центрального. По левому каналу энергия движется, вращаясь против часовой стрелки, а по правому каналу - по часовой стрелке.
Боги-Хранители каналов - Шива и Брахма - имеют в качестве атрибутов свастики, показывающие направление вращения. Система раздельного питания предполагает употребление белков (то есть веществ, имеющих L-конфигурацию) для очищения левого канала и употребление углеводов и жиров (веществ, имеющих D-конфигурацию) для очищения правого канала. Большое внимание также уделяется правильному направлению вращения чакр, которое служит основой здоровья и долголетия.
Интересно, что явление хиральности отражено в древних учениях об организме человека. Так, в системе йоги указано на существование в теле человека трёх каналов - левого, правого и центрального. По левому каналу энергия движется, вращаясь против часовой стрелки, а по правому каналу - по часовой стрелке.
Боги-Хранители каналов - Шива и Брахма - имеют в качестве атрибутов свастики, показывающие направление вращения. Система раздельного питания предполагает употребление белков (то есть веществ, имеющих L-конфигурацию) для очищения левого канала и употребление углеводов и жиров (веществ, имеющих D-конфигурацию) для очищения правого канала. Большое внимание также уделяется правильному направлению вращения чакр, которое служит основой здоровья и долголетия.
Переход от неживой материи к живой произошел, по-видимому после того, как на базе предшественников возникли и развились зачатки двух основополагающих жизненных систем: системы обмена веществ и системы воспроизведения материальных основ живой клетки . В современных организмах обе жизненные системы достигли высочайшего уровня совершенства.
Назначение обмена веществ – поддерживать равновесное состояние живого организма. Такая довольно сложная задача решается путем отбора веществ, из которых синтезируются нужные организму соединения. С другой стороны, эта система выводит из организма все то, что не может быть им усвоено или что появляется как шлак от процессов жизнедеятельности. Система обмена обеспечивает взаимосогласованные биохимические реакции синтеза и расщепления белков.
Система воспроизведения содержит в закодированном виде полную информацию для построения из запасенного клеткой органического вещества нужного в данный момент белка. Она же управляет механизмом извлечения и реализации программной информации. Свои функции система воспроизведения осуществляет посредством полимерных соединений – полинуклеотидов. Здесь ключевая роль принадлежит дезоксирибонуклеиновой кислоте (ДНК) и рибонуклеиновой кислоте (РНК). ДНК хранит генетическую информацию, а РНК воспроизводит ее и переносит в среду, содержащую необходимые для синтеза белка исходные вещества.
В последнее время в изучении механизмов работы основополагающих жизненных систем достигнуты определенные успехи. Но до сих пор никто не знает как же появились эти две системы.
Существует, кроме того, пока необъяснимое, различие физических свойств живого и неживого вещества, отражающее особенность процесса возникновения жизни на Земле. Отличительной особенностью органических соединений, порожденных жизнью, является их оптическая активность – способность поворачивать плоскость поляризации проходящего через них света в одном направлении – либо влево, либо вправо, в зависимости от конкретного типа соединений. Так, все белковые молекулы земных организмов поворачивают плоскость поляризации проходящего света влево, что указывает на их левую пространственную конфигурацию (L-конфигурацию), а молекулы нуклеиновых кислот ДНК и РНК – только вправо, т. е. обладают правой или D-конфигурацией. В то же время неживое вещество подобного химического состава представляет собой смесь с равновероятным содержанием молекул обеих конфигураций, поэтому поворота плоскости поляризации проходящего через них света не происходит. Предполагается, что оптическая активность органических соединений живых организмов имеет прямое отношение к происхождению жизни.
Сохранение в процессах, связанных с жизнью, органических молекул только одной из двух возможных пространственных структур, называют хиральностью , а соответствующие им молекулы – хиральными . Хаотическая же смесь органических молекул обеих пространственных конфигураций называют рацематом , который возникает при абиогенном синтезе органических молекул. Вне сомнений в преджизненный период образования органических соединений на Земле возникал только рацемат. При переходе к жизни в органических соединения вдруг произошла сортировка молекул и появилась хиральность. Существует мнение по поводу возникновения: переход от рацемата к хиральности произошел не в ходе эволюционного, а в результате скачка со всеми характерными чертами самоорганизации материи. Есть другая точка зрения. Ее выдвинул Л. Пастер (1822-1895). Суть ее в том, что зеркальная ассиметрия живых систем следует некоторой ассиметрии Вселенной. Отдавая должное широте взглядов ученого, еще в прошлом веке связавшего жизнь и космос в единое целое, отметим: ассиметрия Вселенной нарушала бы симмерию любого органического вещества, от его происхождения. Точку зрения Пастера пытались развить, выдвигая предположения о существовании каких-то агентов, оказывающих ассиметричное воздействие на вещество организмов. Однако обнаружить таких агентов пока не удалось.
Носитель генетической информации. Нуклеиновые кислоты. Состав и структура молекул ДНК и РНК. Принцип комплиментарности. Геном организма. Свойства генетического кода. Репликация ДНК. Генетические свойства организма.
Дезоксирибонуклеиновая кислота (ДНК) – материальный носитель генетической информации. Это высокомолекулярное природное соединение, содержащееся в ядрах клеток живых организмов. Молекулы ДНК вместе с белками-гистонами образуют вещество хромосом. Гистоны входят в состав ядер клеток и участвуют в поддержании и изменении структуры хромосом на разных стадиях клеточного цикла, в регуляции активности генов. Отдельные участки молекул ДНК соответствуют определенным генам. Молекула ДНК состоит из двух полинуклеотидных цепей, закрученных одна вокруг другой в спираль. Цепи построены из большого числа мономеров четырех типов – нуклеотидов , специфичность которых определяется одним из четырех азотистых оснований: аденин (А), тимин (Т), цитозин (С) и гуанин (G). Сочетание трех рядом стоящих нуклеотидов в цепи ДНК образуют генетический код. Нарушение последовательности нуклеотидов в цепи ДНК приводит к наследственным изменениям в организме – мутациям. ДНК точно воспроизводится при делении клеток, что обеспечивает в ряду поколений клеток и организмов передачу наследственных признаков и специфических форм обмена веществ.
Структурная модель ДНК в виде двойной спирали была предложена в 1953 г. американским биохимиком Дж. Уотсоном и английским биофизиком и генетиком Ф. Криком. За расшифровку генетического кода Дж. Уотсон, Ф. Крик и английский биофизик М. Уилкинс, впервые получивший высококачественную рентгенограмму молекулы ДНК, удостоены Нобелевской премии 1962 г.
ДНК – это удивительное природное образование со спиральной симметрией. Длинные переплетенные нити цепочечной структуры ДНК состоят из молекул сахара и фосфатов. К молекулам сахара присоединяются азотистые основания, образуя поперечные связи между двумя спиральными нитями. Вытянутая молекула ДНК напоминает деформированную винтообразную лестницу. Это действительно макромолекула: ее молекулярная масса может достигать 109. В данных нуклеотидных парах таким образом А всегда связывается с Т, а С с G. Такая связь соответствует принципу комплиментарности .
Способность азотистых оснований к распознаванию своего партнера приводит к свертыванию сахарофосфатных цепей в виде двойной спирали, структура которой экспериментально определена в результате рентгеновских наблюдений.
Сахарофосфатную группу вместе с одним из азотистых оснований А, Т, С или G, образующую нуклеотид, можно представить в виде своеобразного строительного блока. Из таких блоков и состоит молекула ДНК. С помощью последовательности нуклеотидов кодируется информация в молекуле ДНК. В ней содержится информация, необходимая, например, для производства белков, нужных живому организму.
Молекула ДНК может копироваться в процессе катализируемой ферментами репликации, заключающейся в ее удвоении. Процесс репликации включает разрыв старых и формирование новых водородных связей. В начале репликации две противоположные цепи начинают раскручиваться и отделяться одна от другой. В точке раскручивания фермент пристраивает новые цепи к двум старым по принципу комплиментарности, в результате образуются две идентичные двойные спирали. Кодирование генетической информации и репликация молекулы ДНК – взаимосвязанные важнейшие процессы, необходимые для развития живого организма.
Генетическая информация кодируется последовательностью нуклеотидов ДНК. Основополагающие работы по расшифровке генетического кода провели американские биохимики М. Ниренберг, X. Корана и Р. Холли; лауреаты Нобелевской премии 1968 г. Три последовательных нуклеотида составляют единицу генетического кода, называемую кодоном. Каждый кодон кодирует ту или иную аминокислоту, общее число которых равно 20. Молекулу ДНК можно представить в виде последовательности букв-нуклеотидов, образующих текст из большого их числа, например, АСАТ-TGGAG... В таком тексте и содержится информация, определяющая специфику каждого организма. Генетический код всего живого, будь то растение, животное или бактерия, одинаков. Такая особенность генетического кода вместе со сходством аминокислотного состава всех белков свидетельствует о биохимическом единстве жизни, которое, по-видимому, отражает происхождение всех живых существ от единого предка.